Sulfure d'hydrogène (H₂S)
Le sulfure d'hydrogène, H₂S, est un gaz hautement toxique qui a une odeur distinctive et désagréable d'œuf pourri. C'est un gaz incolore, qui peut se produire naturellement dans l'air via diverses sources de pétrole brut ou naturel, des gaz volcaniques et des eaux de source. Des traces de H₂S peuvent être trouvées dans l'atmosphère, ce qui n'est généralement pas nocif.
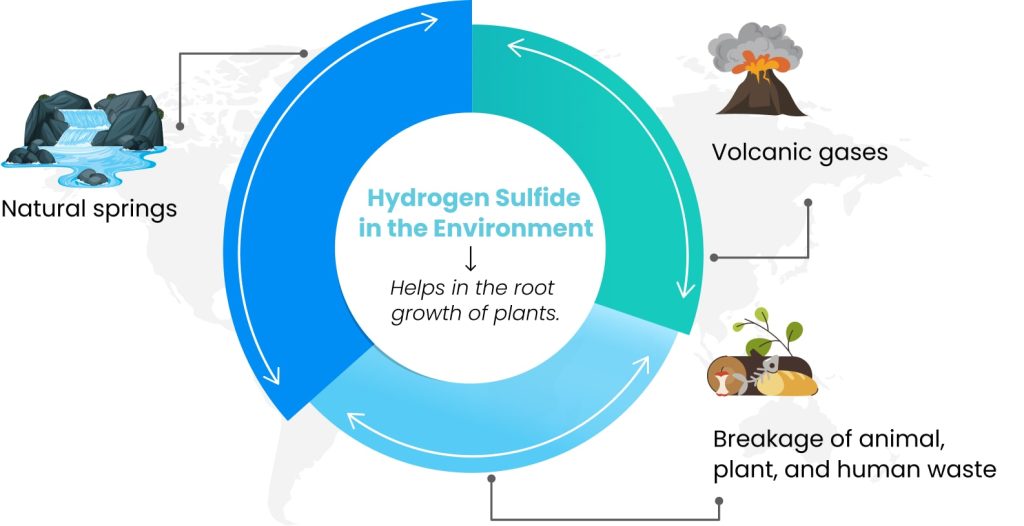
Le sulfure d'hydrogène dans l'environnement
Le sulfure d'hydrogène est produit par la décomposition bactérienne des déchets animaux, végétaux et humains. Il peut également être produit par les gaz volcaniques et les sources naturelles. Le gaz H₂S dissous dans le sol favorise la croissance des racines des plantes.
LE SAVIEZ-VOUS
L'organe cible principal de l'intoxication au sulfure d'hydrogène est le système respiratoire. Une fois inhalé, le sulfure d'hydrogène est rapidement absorbé par les poumons. Cela peut entraîner un arrêt cardiaque ou même la mort car il affecte les tissus neurologiques et cardiaques. Le symptôme le plus connu de l'intoxication au sulfure d'hydrogène est la mort subite chez les égoutiers. Toutes les expositions au H₂S doivent être évitées car elles ont des effets nocifs graves. - Saiyed, H N. Indian Journal of Medical Research ; New Delhi
Sources de sulfure d'hydrogène
Le sulfure d'hydrogène est produit naturellement à partir de la décomposition de la matière organique et des processus industriels, et peut être mortel à des concentrations élevées. Voici quelques-unes de ses sources potentielles :
Sources naturelles

Gaz volcaniques
Pendant l'activité volcanique, les volcans libèrent naturellement du H2S par leurs évents et leurs fissures.

Puits de gaz
Le gaz H2S peut être présent dans les puits de gaz naturel et pourrait être libéré pendant la production et le forage.

Réservoirs de gaz naturel
Il peut être présent dans les réservoirs de gaz naturel et peut être rejeté pendant le traitement et l'extraction.

Sources naturelles
Comme les minéraux contenant du soufre réagissent avec l'eau pour produire du H2S, les sources naturelles peuvent être une source de gaz H2S.

Pétrole brut
Le pétrole brut peut produire du H2S pendant l'extraction et le traitement, ce qui pose des problèmes de santé et de sécurité.
Sources industrielles

Traitement des eaux usées
De la décomposition du contenu organique des eaux usées, les stations d'épuration peuvent émettre du H2S.

Raffineries
Les raffineries peuvent générer du H2S en traitant du pétrole brut contenant du soufre. Le gaz peut constituer une menace pour la santé et la sécurité.
Papeteries Kraft
Dans le processus de mise en pâte, les papeteries kraft utilisent des produits chimiques à base de soufre, qui produisent du H2S comme sous-produit.
Transformation des aliments
Les unités de transformation des aliments qui utilisent des sulfures et de l'acide sulfurique émettent du H2S dans l'environnement environnant.

Traitement des eaux usées
Les stations d'épuration des eaux usées produisent du H2S lors de la décomposition de la matière organique.
Risques pour la santé du sulfure d'hydrogène
Le H2S est extrêmement dangereux pour les travailleurs, les ouvriers, les mineurs, etc. qui doivent travailler avec ce gaz en permanence, de manière régulière. C'est un gaz hautement inflammable qui peut réagir avec l'acier à température ambiante. Cela rend la manipulation, le stockage, le transport et le travail avec le gaz très laborieux et exigeants.

Compte tenu des risques aigus pour la santé des émissions professionnelles de sulfure d'hydrogène, le tableau suivant montre les niveaux de H₂S en PPM par le comité sectoriel de la sécurité industrielle et des risques chimiques.
- Niveaux de H₂S (PPM)
- Durée d'exposition
| 15 min | >15 min | >1h-4h | >4-8ht | |
|---|---|---|---|---|
| 10 | - | - | Irritation des yeux | Concentration maximale tolérable pour une exposition prolongée |
| 50-100 | Perte de la perception olfactive | Irritation des yeux | Irritation des yeux et des bronches | Détresse respiratoire grave et asthénie |
| 150-250 | Irritation des yeux et de la peau | Irritation des yeux et des bronches | Détresse respiratoire grave et asthénie | Danger en cas d'exposition continue |
| 300-400 | Perte de la perception olfactive de l'œil | Détresse respiratoire grave, asthénie aiguë | Œdème pulmonaire et risque de décès | Œdème pulmonaire et risque de décès |
| 500-1,000 | Perte de conscience, détresse respiratoire | Risque d'œdème pulmonaire et de décès | - | - |
- >1,000
- Perte de conscience immédiate et détresse respiratoire
* Selon le BUREAU DES NORMES INDIENNES
Mesures préventives si vous travaillez avec du sulfure d'hydrogène

Surveillez votre espace de stockage
Assurez-vous de surveiller la zone de stockage en temps réel afin que tout déversement ou fuite puisse être identifié et que des stratégies immédiates puissent être adoptées.
Gardez un œil sur la température
Maintenez la température où le gaz est stocké car une température plus élevée peut décomposer les éléments gazeux, ce qui peut provoquer l'éclatement du conteneur de stockage.

Ne pas fumer près de la zone de stockage
La zone où le gaz est stocké doit être une ZONE NON-FUMEUR car le gaz est hautement inflammable. Une petite étincelle peut être mortelle s'il y a du sulfure d'hydrogène dans l'air.
La ventilation est la clé
La zone doit être très bien ventilée. Le sulfure d'hydrogène est plus lourd que l'air. Il peut facilement se déplacer vers n'importe quelle source d'inflammation. C'est pourquoi la ventilation est importante dans les zones de stockage.

Utiliser des mesures de précaution
Un équipement de protection doit être utilisé lors de la manipulation du gaz, tel que des lunettes de sécurité, des vêtements étanches à l'air, un équipement de protection respiratoire, etc. Évitez tout contact direct avec la peau.
Sécurité incendie prête à l'emploi
Gardez un extincteur à portée de main en cas d'accident. Il y a de fortes chances d'incendie car le sulfure d'hydrogène est hautement inflammable.
Comment détecter le gaz H₂S
Un moniteur/capteur de qualité de l'air peut détecter le gaz H2S et fournir des informations en temps réel sur sa concentration dans l'air. Ces données peuvent aider à prendre des décisions éclairées pour protéger la santé publique et l'environnement.